Cell Rep丨侯盼盼/郭德银/李春梅团队揭示抗流感病毒新机制
2026-05-0153流感病毒感染宿主细胞后,需要经历一系列精密而高度协调的步骤,其中“脱壳”(uncoating)是启动病毒复制的关键环节。在这一过程中,病毒包裹的核糖核蛋白复合体(vRNP)从病毒颗粒中释放,并被转运进入细胞核,从而启动病毒基因组复制与转录。尽管该过程对于病毒生命周期至关重要,但其调控机制长期以来仍未被完全阐明。近日,实验室联合联合广州实验室、中山大学等单位在Cell Reports发表重要研究成果: Ubiquilin1 restricts influenza viral replication through trapping vRNP in the late endosomes,系统揭示了宿主蛋白Ubiquilin1(UBQLN1)通过调控病毒早期关键步骤,从源头阻断流感病毒复制的全新机制。该研究不仅深化了对流感病毒感染过程的认识,也为开发新型广谱抗病毒策略提供了重要理论基础。

该研究通过系统筛选与功能验证,首次鉴定UBQLN1为一个关键的宿主抗流感病毒因子。在细胞水平上,UBQLN1缺失显著增强流感病毒复制,而其过表达则明显抑制病毒扩增。在体内实验中,Ubqln1敲除小鼠表现出更高的病毒载量、更严重的肺组织损伤以及更低的生存率,充分证明UBQLN1在抗流感感染中的重要生理功能。机制研究进一步揭示,UBQLN1通过一种不同于传统抗病毒途径的方式发挥作用。传统抗病毒机制多依赖于降解病毒蛋白或抑制病毒酶活性,而UBQLN1则主要通过“空间限制”策略干预病毒生命周期。具体而言,UBQLN1能够直接结合病毒vRNP复合体,并在晚期内体阶段阻断其脱壳过程。研究发现,UBQLN1通过干扰宿主蛋白HDAC6与病毒M1蛋白之间的相互作用,抑制病毒外壳解离,从而阻止病毒vRNP的释放。此外,UBQLN1还通过第二重机制进一步增强其抗病毒效应。对于少量成功释放的vRNP,UBQLN1能够干扰其与核转运蛋白importin的结合,从而抑制其进入细胞核。这种“双重封锁”机制使病毒在复制早期即被有效阻断,大幅降低感染效率 (图 1)。UBQLN1并非通过“消灭病毒”,而是通过“限制病毒空间位置”来抑制其复制,提出了“空间性抗病毒调控”的新理论。这一机制拓展了人们对宿主抗病毒策略的理解,为探索新的抗病毒调控路径提供了重要启示。
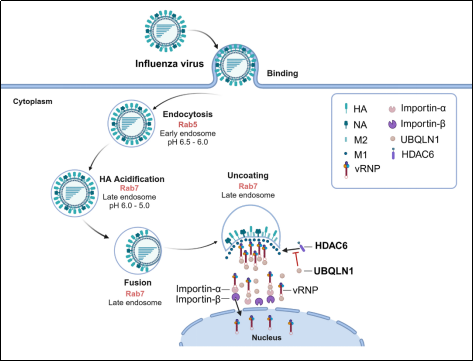
图1:UBQLN1调控流感病毒脱衣壳与vRNP入核过程
值得注意的是,UBQLN1的抗病毒作用具有广谱性。该研究表明,其不仅能够抑制经典H1N1病毒,还对H3N2和H9N2等多种流感病毒亚型具有显著抑制作用。这一发现提示,UBQLN1可能代表一种保守的宿主防御机制,具有开发为广谱抗流感策略的潜力。从应用角度来看,该研究提出了一种全新的抗病毒干预思路。当前主流抗流感药物主要靶向病毒自身蛋白,容易因病毒突变而产生耐药性。而以UBQLN1为代表的宿主靶向策略,则通过干预病毒依赖的细胞过程实现抑制,理论上更难产生耐药,同时具备更广泛的适用性。此外,由于UBQLN1作用于病毒复制的最早阶段,其干预可能在感染初期即发挥效果,从而显著提高治疗窗口。综上所述,该研究首次揭示UBQLN1通过在内体中滞留病毒核糖核蛋白复合体并阻断其核转运,从而在病毒复制最早阶段实现精准抑制,不仅丰富了流感病毒感染机制的理论体系,也为开发新型宿主靶向抗病毒药物提供了重要方向。
广州国家实验室-中山大学联培博士生郑碧荣,广州医科大学博士后王朝焕和广州医科大学冉伟教授为该文的共同第一作者,研究得到中山大学医学院张辉教授、广州医科大学赵金存教授的支持,广州国家实验室郭德银教授、实验室侯盼盼教授与中山大学医学院李春梅教授为该文的共同通讯作者。该研究得到了国自然重大研究计划、广州实验室专项等项目资助。