李靖教授团队在AAIR发表综述文章:环境暴露免疫应答在过敏性哮喘进程中的重要作用
2020-07-274850近日呼吸疾病国家重点实验室、广州呼吸健康研究院哮喘与呼吸免疫研究团队在韩国过敏与哮喘领域杂志Allergy, Asthma and Immunology Research (AAIR) 发表综述性文章“Important Role of Immunological Responses to Environmental Exposure in the Development of Allergic Asthma”。广州医科大学林新鎏硕士为第一作者,李靖教授和苏钟教授为共同通讯作者。
近年来哮喘的患病率显著增加,在发达国家尤为明显,且城市高于农村。由于人类遗传背景的变化有限,环境可能是主因。“卫生假说” 认为,过度清洁的环境将导致哮喘等过敏性疾病(包括湿疹和花粉症)的患病率上升。这篇综述重点关注农场和农村地区的环境在减少哮喘发病的作用,其中微生物和病原相关分子模式(PAMP)是重要的环境因素,可调节宿主的先天和适应性免疫系统,从而产生保护效应。本文也讨论了环境微生物相关的免疫疗法将是未来研究哮喘防治策略的新方向。
过敏性哮喘的流行病学趋势
自1950年以来,全球过敏性哮喘的患病率呈上升趋势。《国际儿童哮喘与过敏研究》(ISAAC)平均间隔7年对过敏性哮喘、过敏性鼻结膜炎和湿疹的多中心调查数据表明,三种过敏性疾病均有增加。总体上,发达国家的哮喘患病率较高。同时,在经济快速增长和城市化的发展中国家,哮喘患病率也显著增加。
与城市相比,农村的哮喘患病率相对较低。在欧洲,农场和农村环境被认为是对抗哮喘的两个经典保护因素。我们的研究表明,从化农村地区儿童的哮喘患病率明显低于广州城市地区的儿童(分别为3.4%和6.9%)。两组儿童的变应性鼻炎和湿疹患病率也显示出相似的城乡差异。与华南地区的情况类似,华北农村地区儿童的哮喘患病率明显低于北京城市(分别为1.1%和6.3%)。
环境和微生物暴露与哮喘
环境暴露与哮喘
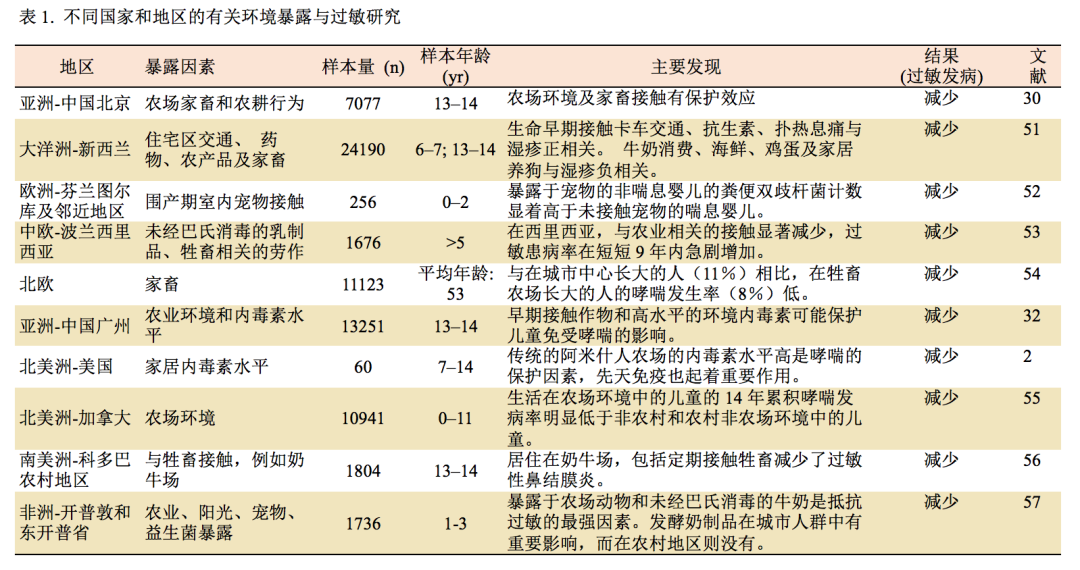
大量的欧洲农场、美国传统和现代农场对照研究提示,在农场长大的儿童的过敏性体质和过敏的风险显著低于在非农场长大的儿童,这种保护作用被称为“农场效应”。在中国的南部和北部地区,我们还发现农业环境和农村室内灰尘内毒素可减少儿童哮喘。由于环境的多样性,在不同的研究中发现了多种保护性环境因素,我们将近年来在不同地区研究的主要发现总结于表1。
微生物暴露与哮喘
微生物及其成分可能在调节过敏性疾病(例如哮喘)中发挥关键作用。农场的洛菲不动杆菌和乳酸乳球菌可诱导Th1细胞分化,并减轻过敏性气道炎症。室内灰尘中的细菌和真菌衍生物暴露与儿童哮喘发病显著负相关。当非农业家庭室内细菌组成与农场室内的构成相似时,其儿童长大后患哮喘的风险降低。
此外,农场和农村环境中高水平的内毒素与哮喘等过敏的患病率负相关。内毒素可能诱导肺上皮细胞中A20表达,通过调节儿童的先天免疫途径预防哮喘。除了内毒素外,许多病原体相关的分子模式(PAMPs),如胞外多糖(EPS),胞壁酸和葡聚糖也已被证明与农场的保护作用密切相关。
孕期或生命早期抗生素暴露、抗寄生虫治疗、剖宫产,减少了婴幼儿与微生物接触的机会,可增加儿童哮喘发病。同时要注意某些类型的微生物可能加重哮喘,例如感染肺炎链球菌、流感嗜血杆菌和卡他莫拉菌。
哮喘的环境因素与免疫调控
哮喘涉及固有免疫和适应性免疫。促进或抑制哮喘发作的常见因素包括过敏原暴露、微生物和寄生虫感染、氧化应激、环境及微生物相关代谢产物接触。参与此过程的细胞种类繁多。图1介绍了促进和抑制哮喘涉及的环境因素和免疫调节机制。
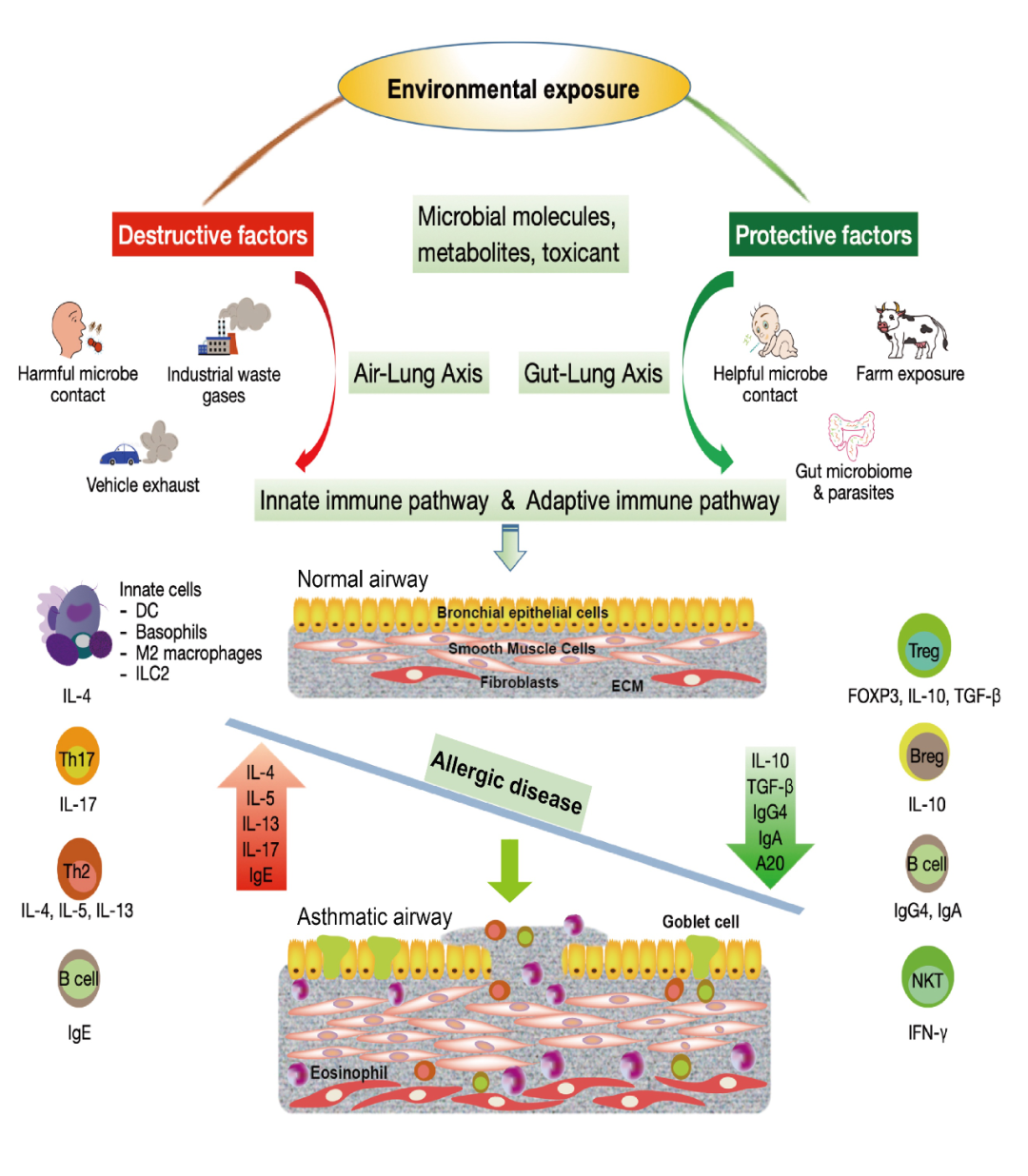
图1.环境因素影响过敏性哮喘的潜在免疫学机制
环境微生物分子和代谢物通过气肺轴和/或肠肺轴作用于先天性和适应性免疫途径,以发挥其免疫调节作用。有害细菌、病毒和工业废气以及汽车尾气会通过先天免疫细胞(例如ILC2、气道上皮细胞、树突状细胞、巨噬细胞和嗜碱性粒细胞)和适应性免疫细胞(例如Th17细胞,Th2细胞和B细胞),诱导白介素(IL)-4,IL-5,IL-13,IL-17分泌来促进气道炎症导致气道粘膜损伤、平滑肌增生和纤维化。相反,保护性环境因素,例如早期与有益微生物接触、肠道寄生虫感染、肠道菌群和农场暴露等,可能导致产生IL-10、转化生长因子β(TGF-β)、干扰素-γ(IFN-γ)、免疫球蛋白A和G4(IgA、IgG4)通过先天性(TLR、气道上皮、DC、NKT细胞)和适应性免疫细胞(Tregs、Bregs和B细胞)来防止过敏性哮喘。
先天性免疫机制
Toll样受体(TLR)被认为是调节免疫应答的关键系统,暴露于农场的儿童的CD14 /TLR2表达水平增加;孕妇在分娩前暴露于富含微生物的环境会导致其子女的先天免疫系统受体(即TLR2、TLR4和CD14)的基因表达水平升高;孕妇分娩前接触家畜会导致儿童脐带血中TLR5和TLR9显着增加,而特应性皮炎的风险显著降低。适当浓度的脂多糖(LPS)暴露会削弱过敏相关信号通路、增加锌指蛋白A20合成,从而抑制哮喘。与现代农场比较,传统农场儿童的血嗜酸性粒细胞百分比下降,单核细胞表现出抑制性表型(HLA-DR和更高水平的ILT3)。此外,传统的农场粉尘提取物在哮喘动物模型中具有显著的保护作用,且该作用依赖于先天免疫系统。
某些PAMPs可以不依赖TLR直接激活iNKT细胞某些亚群,进而抑制哮喘。幼年小鼠甲流感染可以减轻成年鼠气道高反应性(AHR),且与NKT细胞亚群相关。早期/新生儿感染或抗原刺激可在肺中诱导某些NKT亚群(例如CD38hiDN NKT细胞)产生IFN-γ,但不产生IL-17、IL-4或IL-13,从而阻断变应原诱导的AHR。
获得性免疫机制
Gereda等人的研究表明持续暴露于环境内毒素会诱导Th1免疫应答,从而改变Th1 / Th2平衡,继而降低过敏患病率。感染钩虫或鞭虫的哮喘小鼠可分泌抗炎蛋白2(AIP-2)和蛋白P43,通过与IL-13结合抑制过敏。
调节性T细胞(Tregs)在哮喘的免疫调节、平衡T细胞的分化和成熟中有重要作用。McGuirk和Wilson等报道细菌和蠕虫感染可以促进Treg细胞的发育。Schaub等发现母体农场暴露可调节儿童的免疫系统、增加新生儿脐带血中Treg的数量和功能、减少Th2淋巴细胞的增殖。母亲食用牛奶可能会增加孩子的FoxP3去甲基化,从而降低孩子在儿童期和成年期患哮喘的风险。我们发现小鼠感染肠道多形螺旋线虫(H. polygyrus) 引起Breg细胞的显著应答,进而促进Treg细胞的分化和增殖,从而抑制哮喘。
怀孕期间与家畜或猫接触可能会增加母乳中sIgA的水平并减少其子女的特应性皮炎。许多研究表明,母乳中sIgA和TGF-β水平的升高对儿童哮喘有保护作用。动物实验也表明,线虫的可溶性提取物可以增加IL-10和TGF-β的水平,从而抑制哮喘中的气道炎症。
未来研究方向
我们需要进行更多的队列观察,以确定微生物暴露的“最佳时间窗口”,并鉴定具保护效应的微生物。且仍需要进行更多的干预研究,进一步阐明哮喘发病中的分子机制。此外,微生物免疫疗法已尝试作为预防过敏性哮喘的潜在手段,因此,需要深入研究以明确有益及有害微生物,从而合理安全地用于控制哮喘和其他过敏性疾病。