王涛、洪城教授团队发现GP IIb/IIIa-ICAM-1介导的血小板-内皮黏附加重肺动脉高压
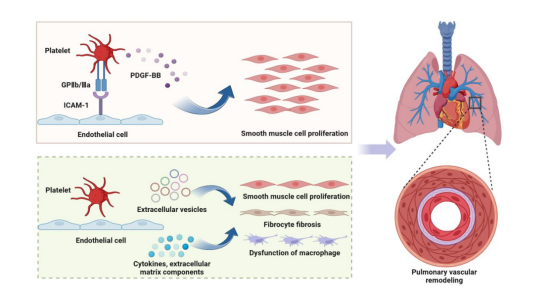
2025-03-2123072025年3月20日,王涛教授、洪城教授团队在呼吸病学领域权威期刊《American Journal of Respiratory Cell and Molecular Biology》(JCR分区:Q1,影响因子:5.9)在线发表了一篇题为《GP IIb/IIIa-ICAM-1 Mediated Platelet-Endothelial Adhesion Exacerbates Pulmonary Hypertension》的研究论文。该研究首次揭示了血小板通过糖蛋白IIb/IIIa(GP IIb/IIIa)与内皮细胞间黏附分子-1(ICAM-1)的相互作用介导血小板-血管内皮黏附,激活血小板并释放血小板源性生长因子BB(PDGF-BB),从而促进肺动脉平滑肌细胞(PASMC)增殖和迁移,最终加剧肺血管重塑及肺动脉高压(PH)进展的分子机制。研究进一步提出,靶向抑制GP IIb/IIIa或ICAM-1可显著改善PH病理进程,为PH的精准干预提供了新靶点。

研究背景:血小板功能异常与肺动脉高压的未解之谜
肺动脉高压(PH)以进行性肺血管重塑和右心衰竭为特征,死亡率居高不下,亟需揭示新的病理机制以突破治疗瓶颈。临床观察发现,PH患者普遍存在血小板减少,且血小板参数(如平均体积、分布宽度)与疾病严重程度相关,但其病理意义尚未明确。既往研究提示,血小板可能通过释放生长因子(如PDGF-BB)或介导微血栓形成参与肺血管重构,但这些过程是否依赖于特定分子互作仍存在争议。值得注意的是,动物模型中单纯调控血小板数量(如输注或清除)对PH表型的影响呈现矛盾结果,提示血小板功能异常可能独立于数量变化驱动疾病。基于此,本研究聚焦于血小板-内皮交互作用,旨在解析GP IIb/IIIa与ICAM-1介导的黏附通路如何调控血小板活化及促增殖因子释放,从而为PH治疗提供精准干预靶点。
创新发现:GP IIb/IIIa-ICAM-1介导的血小板-内皮黏附促进PH进展
1、血小板功能主导PH进程:输注PH模型动物血小板可使健康动物肺血管增厚,而健康血小板则缓解PH;同时,单纯增加PH动物内源性血小板数量对疾病表型影响有限,提示血小板功能异常是关键。
2、关键分子机制:PH患者血小板中GP IIb/IIIa(ITGA2B/ITGB3)表达显著上调,通过结合肺血管内皮ICAM-1增强黏附,触发血小板活化及PDGF-BB释放,进而促进PASMC增殖和迁移。
3、靶向干预效果:GP IIb/IIIa拮抗剂(如替罗非班)或ICAM-1抑制剂(A-205804)可显著减少血小板-内皮黏附,抑制PDGF-BB分泌,并改善动物模型中的肺血管重塑和血流动力学指标。
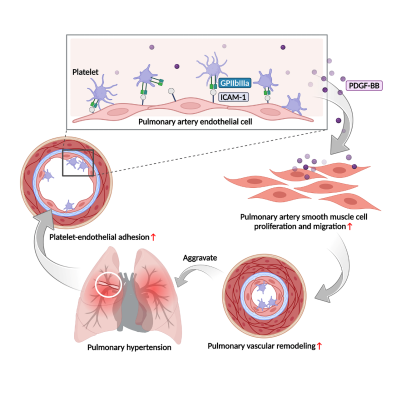
研究意义
本研究通过整合临床样本分析与动物模型实验,首次详细地阐明了血小板功能异常(而非数量变化)在肺动脉高压(PH)进展中的核心作用。为PH治疗提供了新的治疗靶点并拓宽了治疗方案,在现有的用药选择上对增加对血小板的干预可能增强现有治疗措施的疗效,从而进一步降低PH相关的死亡率,提高患者的生活质量。
致谢
该研究得到了国家自然科学基金面上项目、广东省自然科学基金杰出青年基金、广州市科技计划项目的支持。
关于研究团队
实验室王涛教授和洪城教授为本研究共同通讯作者,陈灵丹博士、白茜文硕士研究生和唐瑞娣博士研究生为共同第一作者。本研究依托呼吸疾病全国重点实验室平台完成。
文章发表后,杂志配发了南京医科大学陈峰教授(国家自然科学杰出青年基金获得者)为本研究撰写的专题Editorial,评论该研究“为血小板在PH发病机制中的作用提供了有力证据,表明靶向干预血小板可能为PH提供新的治疗益处。”