美国癌症协会会刊《Cancer Research》在线发表实验室肺癌肿瘤代谢调控研究新成果
2019-03-223377近期,国际知名学术期刊、美国癌症协会会刊《Cancer Research》在线发表了实验室与天津医科大学医学院、上海交通大学医学院有关“肺癌肿瘤代谢调控研究”的合作研究成果:“PAK4 phosphorylates fumarase and blocks TGF-β-induced cell growth arrest in lung cancer cells”。研究阐明了转化生长因子β(TGF-β)刺激下,延胡索酸水合酶(FH)偶联p53和Notch信号通路,调控表观遗传介导细胞生长阻滞的机制;发现在非小细胞肺癌(NSCLC)中,p21活化蛋白激酶4(PAK4)对这一机制产生抑制,从而促进肿瘤细胞的生长增殖。
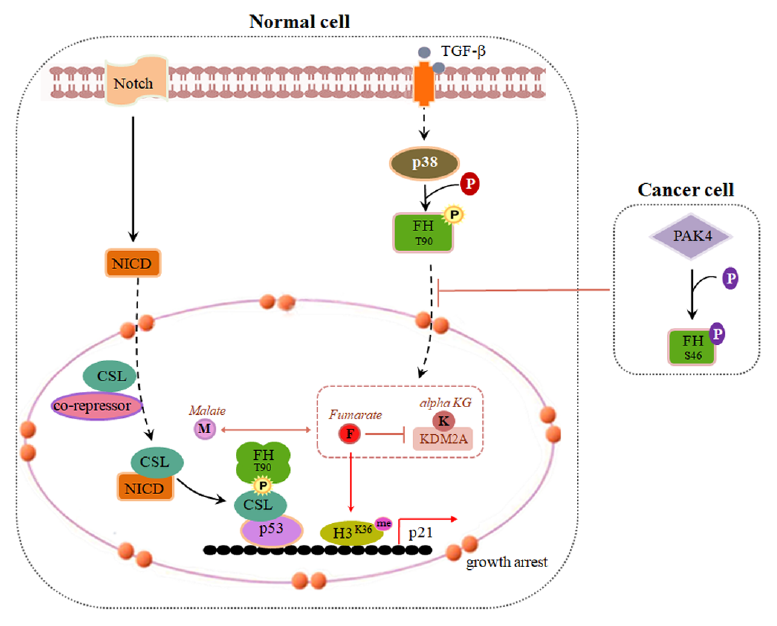
非小细胞肺癌患者占肺癌患者总数的80%以上,且恶性程度高,多数患者确诊时已为中晚期,患者5年生存率仅为21%。非小细胞肺癌对药物具有固有抗性和获得性抗性,使患者临床治疗效果不佳;因此急需针对NSCLC特征,寻找新的、有效的诊断治疗靶点。
细胞代谢发生异常重编程是肿瘤发生的重要原因。代谢酶FH在细胞内可利用其酶活性调控组蛋白表观修饰,进而调控基因表达影响细胞生命活动。p53是细胞内的抑癌因子,可介导细胞生长阻滞和细胞凋亡,其功能缺失在多数肿瘤细胞中较常见。据报道,TGF-β信号通路的激活可促使p53发挥抑癌功能。同时经报道,Notch通路的效应分子CSL可抑制p53介导的细胞衰老。基于这些依据,作者开始探索Notch信号通路和TGF-β信号通路的交互作用对p53功能的调控,以及FH在其中所扮演的角色。
研究人员首先发现在TGF-β的刺激和Notch通路激活下,FH的90位苏氨酸可被p38磷酸化并与CSL-p53形成复合物,从而被招募到p21启动子处;且此过程对TGF-β介导的细胞生长阻滞必不可少。同时,FH酶活突变型与野生型对照实验、外源延胡索酸添加等实验表明,FH催化活性及其在细胞核内产生的延胡索酸可抑制KDM2活性,维持组蛋白H3的36位赖氨酸甲基化水平,这对于TGF-β介导的细胞生长阻滞必不可少。进一步研究发现,在非小细胞肺癌细胞中,FH的46位丝氨酸被PAK4磷酸化后与14-3-3蛋白结合,抑制了FH-CSL-p53复合物的形成,促进肿瘤细胞生长增殖。最后,研究人员在小鼠体内和临床样本层面验证了上述机制。该研究结果为临床非小细胞肺癌的精准诊治提供了新的理论基础。
该研究论文第一作者为实验室陈涛博士、梁文华博士及天津医科大学王霆教授,通讯作者为实验室何建行教授、上海交通大学医学院蒋玉辉教授。感谢钟南山院士自研究伊始的亲自指导、关心与支持,感谢呼吸疾病国家重点实验室自主/开放课题基金、国家自然科学基金项目的资助。
论文链接:
http://cancerres.aacrjournals.org/content/early/2019/02/15/0008-5472.CAN-18-2575